מחלת SMA (מחלת ניוון שרירים שדרתית) היא מחלה ניוונית תורשתית נדירה הפוגעת בחלק של מערכת העצבים השולט בתנועות שרירים רצוניות. ללא טיפול, המחלה פוגעת בהדרגה בתפקוד של שרירי הגוף, בהם השרירים האחראים על תנועה, אכילה וגם נשימה.
במחלת SMA חל אובדן של תאים חשובים בחוט השדרה הנקראים תאי עצב (נוירונים) מוטוריים, החיוניים לחוזק ותנועת השרירים. נוירונים מוטוריים אלה מווסתים את פעילות השרירים על ידי שליחת אותות ממערכת העצבים המרכזית (CNS) שהיא החלק של מערכת העצבים הכולל את המוח וחוט השדרה.
אובדן של נוירונים מוטוריים מוביל לחולשת שרירים מתקדמת, רפיון שרירים (היפוטוניה) ולדלדול השרירים (אטרופיה) עקב ירידה הדרגתית במסה ובחוזק של השרירים ובמתח שלהם, כאשר השרירים מפסיקים לקבל אותות מה-CNS.
בניגוד להרבה מחלות נוירו-שריר נדירות אחרות, ישנה הבנה ברורה של הגורם הגנטי הספציפי למחלת SMA.
המחלה נגרמת כתוצאה ממוטציה שמשבשת את תפקודו של גן הנקראSMN1 . גן זה כולל את הוראות הייצור, או "המתכון", של חלבון הנקרא Survival Motor Neuron -SMN שאחראי לתפקוד התקין של תאי העצב המוטוריים – שתפקידם לקבוע את פעולת שרירי הגוף.
בחולי SMA המוטציה גורמת לפגיעה בייצור החלבון, ובלעדיו העצבים השולטים בשרירים לא יכולים לתפקד כראוי. תאי עצב אלה מתנוונים ומתים בהדרגה, וכתוצאה מכך נוצרת חולשת שרירים מתקדמת שמביאה לנכות ועלולה גם לגרום למוות ללא טיפול מתאים.
בעבר, חולי SMA סווגו לתתי-סוגים (TYPE1,2,3,4) של המחלה בהתאם לגיל בו תסמיני המחלה הופיעו לראשונה ומידת המוגבלות הפיזית שהיא גרמה להם.
כיום, עם אפשרויות הטיפול המתרחבות אשר משנות את מהלך המחלה והיכולת לאבחן את החולים כבר בלידה, חלוקה זו הפכה לבלתי רלוונטית. לכן המלצות לניהול המחלה בשלב השיקום מבוססות על חלוקה לפי רמת הניידות הנוכחית של החולים: הולכים/ יושבים/ לא יושבים.
מחלת ה SMA משפיעה על כל אחד בצורה שונה, וחשוב לציין שהתסמינים יכולים להשתנות מאוד בהתאם לגיל ההופעה וחומרת המחלה. חולים יחוו חולשת שרירים מתקדמת בשרירים הקרובים ביותר למרכז הגוף, כגון שרירי הגו, הכתפיים, הירכיים והאגן. שרירים אלו מאפשרים פעילויות כגון שליטה על הראש, ישיבה, זחילה והליכה. תפקודי הנשימה והבליעה עשויים להיות מושפעים גם הם.
מחלת SMA כאמור משבשת את תפקוד העצבים השולטים בשרירי הגוף ויכולה לגרום לפגיעה חמורה ביכולת הפיזית, אולם אין למחלה כל השפעה על תאי עצב אחרים או על התפקוד הקוגניטיבי של החולים, וההתפתחות השכלית והרגשית שלהם אינה שונה מזו של כל אדם בריא.
תסמינים מוקדמים למחלה יכולים להופיע מייד לאחר הלידה, או במקרים אחרים תסמינים יופיעו בגילאים שונים לאחר שלא הושגו אבני דרך בהתפתחות.
חשדם של הורים יכול להתעורר כאשר התינוק או הילד אינו משיג את אבני הדרך בהתאם לגילו. למשל, תינוק שנראה רפוי עם טונוס שרירים נמוך, עם חוסר יכולת להרים את הראש, תנועה מוגבלת בידיים וברגליים, חוסר יכולת לזחול, לשבת באופן עצמאי, לעמוד וללכת. לעיתים כבר בשבועות הראשונים לחיי התינוק ניתן להבחין בנשימה מהירה ושטחית ובקשיי בליעה. מומלץ לפנות לברור רפואי.
ההשלכות של SMA משתנות בין אדם לאדם בהתאם למידת הפגיעה וחומרתה. לעתים קרובות חייהם ועצמאותם של אנשים עם SMA מושפעים מאוד מתסמינים שונים ובהם חולשת שרירים, סיבולת מופחתת, עייפות וכאב אשר מקשים על המטופלים לבצע משימות יומיומיות. בשל אתגרים אלו, חולים ובני משפחותיהם עלולים לחוות עומסים פיזיים, פסיכולוגיים, חברתיים וכלכליים.
בנוסף לאובדן התפקודים המוטוריים, להשלכות אחרות יש השפעה על איכות החיים של הנפגעים. בין אלה הם:
מחלת ה SMA שייכת לקבוצת המחלות התורשתיות הנגרמות כתוצאה מפגיעה בתפקוד של גן יחיד (מחלות מונוגניות). אצל חולי SMA הפגיעה מתמקדת בגן שנקרא SMN1 ראשי תיבות של Spinal Motor Neuron 1.
הגן מכיל את הוראות ההפעלה לייצור של חלבון SMN שאחראי לתפקוד התקין של תאי העצב השולטים בפעולת שרירי הגוף.
כשהגן SMN1 פגוע ולא מתפקד – לא מיוצר החלבון SMN ולא מועברות פקודות לתאי העצב השולטים בשרירי הגוף.
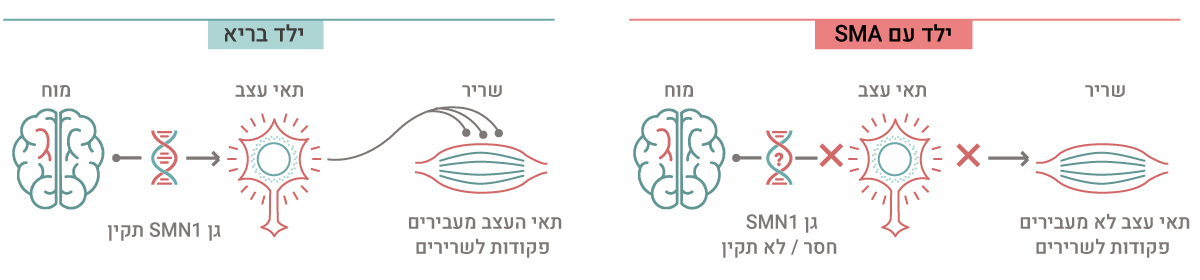
ברוב המכריע של המקרים, המחלה מופיעה כאשר שני ההורים נשאים, והילד או הילדה יורשים עותק פגום של הגן מכל אחד מהוריהם.
בסביבות 1 מכל 40 עד 50 בני אדם בעולם הוא נשא של SMA. ללא קשר לגזע, מין או עדה.
לילד שנולד לשני הורים נשאים יש 25% סיכוי לקבל שני עותקים פגומים של הגן ולפתח את המחלה, 50% סיכוי להיות נשא בעצמו (עם גן יחיד לא תקין) ו-25% סיכוי לקבל את שני העותקים התקינים של הגן – אחד מכל אחד מהוריו.
מכיוון שלנשאות אין כל השפעה בריאותית על הנשא, עד לשנים האחרונות במרבית המקרים גילוי הנשאות התרחש לאחר שנולד ילד שאובחן עם SMA. אולם כיום, בדיקות נשאות ל-SMA כלולה בסל התרופות ומוצעת במסגרת סל הבריאות לכל זוג המתכנן הריון בישראל והיא ניתנת בחינם במסגרת ייעוץ גנטי הניתן בקופות החולים.
במקרה ששני ההורים נשאים, ניתן לבצע בדיקת סיסי שליה או מי שפיר לבדיקת העובר בשלבים הראשונים של ההריון או לחלופין לתכנן את ההריון ולערוך ברירת עוברים (PGD) כדי להבטיח שלא ייוולד ילד חולה.
מסיבה זאת, על אף שסל הבריאות כולל בדיקת אחד ההורים בלבד, העמותה ממליצה לבצע בדיקה גנטית לנשאות SMA לשני ההורים כדי לשלול נשאות אצל מי מהם ולבדוק טוב בעזרת יועץ גנטי את ההיסטוריה הגנטית המשפחתית
לכל האנשים עם SMA יש לפחות "גן גיבוי" אחד, המכונה SMN2. לגן SMN2 יש מבנה דומה ל-SMN1, אך רק כמות קטנה (10%) מהחלבון SMN שהוא מייצר מתפקדת במלואה. רמה נמוכה זו של חלבון SMN אינה יעילה מספיק כדי לקיים את הישרדותם של נוירונים מוטוריים במערכת העצבים המרכזית.
מספר העתקים של SMN2 עשוי להשתנות, ומספר עותקי SMN2 גבוה יותר קשור לתסמינים פחות חמורים של ניוון שרירי עמוד השדרה. אף על פי כן, למחלה מגוון רחב של תסמינים וקשה לחזות את חומרתה על סמך מספר עותקי ה-SMN2 בלבד. לפיכך, מומחים ממליצים לקבל החלטות טיפוליות על סמך יכולתו התפקודית של הפרט ולא על סמך מספר העתק SMN2 בלבד.
הגיבוי הגנטי גם מהווה בסיס לטיפולים חדשים שפותחו עבור החולים עם SMA. גישה רפואית אחת שהראתה הצלחה בפיתוח טיפולים לחולי SMA מתמקדת בעידוד הגן SMN2 לייצר כמות גדולה יותר של החלבון. גישה אחרת משפיעה על תהליך התרגום של הגן לחלבון כדי שידמה יותר לאופן הפעולה של הגן SMN1. גישה שלישית רותמת את כלי העריכה הגנטית כדי לתקן את SMN1 ישירות.
בDNA של מרבית בני האדם יש שני עותקים תקינים של הגן SMN1. נשאי SMA הם בני אדם עם עותק אחד תקין ועותק אחד פגום של הגן. אצל נשאים, העותק התקין מבטיח ייצור מספיק של החלבון החיוני בגוף והנשאות לא משפיעה כלל על בריאותו של הנשא.
מחלת הSMA מתפתחת רק כאשר שני העותקים של הגן פגומים.
קיים מצב נדיר בו לאחד ההורים יש שני העתקים של הגן SMN1 אולם שניהם נמצאים על אותו כרומוזום ואילו הכרומוזום השני אינו מכיל כלל את הגן. במקרה זה ההורה יהיה נשא כי עלול להוריש לצאצא שלו את הכרומוזום עם הגן הפגום. במקרה נדיר זה ההורה לא יאובחן בבדיקה הנשאות כנשא מכיון שהואבעל 2 העתקים של הגן. מצב זה נקרא נשאות סמויה.
מסיבה זאת, על אף שסל הבריאות כולל בדיקת אחד ההורים בלבד, העמותה ממליצה לבצע בדיקה גנטית לנשאות SMA לשני ההורים כדי לשלול נשאות אצל מי מהם ולבדוק טוב בעזרת יועץ גנטי את ההיסטוריה הגנטית המשפחתית
כמו כן, ב-1 מכל 20 נשאים של של עותק פגום של SMA, הפגיעה נגרמת כתוצאה משינוי גנטי (מוטציה) זעיר מכדי שיזוהה בבדיקות הסקר הקיימות כיום. מדובר בפגם גנטי הנוצר אצל האדם עצמו, מסיבה שעדיין אינה ברורה, ובלי שהוא ירש את הגן הפגום מהוריו.
ייתכנו גם מקרים נדירים ביותר בהם מתפתחת המחלה כאשר רק אחד מההורים הוא נשא, אולם גם העותק שהילד או הילדה קיבלו מההורה השני הוא פגום, כנראה כתוצאה ממוטציה שנוצרה בעת התפתחות הביצית או הזרעון.
מסיבה זאת, על אף שסל הבריאות כולל בדיקת אחד ההורים בלבד, העמותה ממליצה לבצע בדיקה גנטית לנשאות SMA לשני ההורים כדי לשלול נשאות אצל מי מהם ולבדוק טוב בעזרת יועץ גנטי את ההיסטוריה הגנטית המשפחתית
בדיקה גנטית היא הדרך המדויקת ביותר לאשר אם לאדם יש את המוטציה בגן SMN1 שגורמת ל-SMA.
הטיפול ב- SMA עבר שינוי תפיסתי גדול בשנים האחרונות. בעבר, בהעדר תרופות הטיפול ב-SMA התמקד אך ורק בניהול המחלה; כיום, ישנן תרופות פורצות דרך וחדשניות העשויות לשנות את מהלך המחלה והחולים יכולים לראות שיפור משמעותי ביכולות התפקוד שלהם.
ככל שהאבחון והטיפול מוקדמים יותר – אפילו לפני הופעת הסימנים הקליניים – כך ניתן למנוע את נזקי המחלה, שכן SMA היא מחלה מתקדמת ואובדן של הנוירונים המוטוריים הוא בלתי הפיך.
לפי הערכות, אחד מכל 40 עד 50 ישראלים הוא נשא SMA – שאחד משני עותקי הגן SMN1 ב-DNA שלו הוא פגום. לנוכח שכיחות הנשאות וחומרת המחלה, משרד הבריאות ממליץ כיום לכל זוג המתכנן להביא ילדים לעולם לערוך בדיקה לנשאות של SMA במסגרת הבדיקות הגנטיות שהם עורכים לפני הכניסה להריון או עד השבוע ה-13 להריון, גם אם אין במשפחה היסטוריה של מחלות תורשתיות.
הבדיקה נעשית בעזרת דגימת דם שנלקחת מהאם או האב לעתיד. במקרה בו היא או הוא מזוהה כנשא/ית, תיערך בדיקה מקבילה גם בדמו של ההורה השני לעתיד.
עם זאת, חשוב לציין כי לבדיקות המשמשות כיום לזיהוי נשאות לSMA ישנן כמה מגבלות. בדיקות הסקר לא מאפשרות כיום לזהות מקרים של "נשאות סמויה", ומקרים נדירים שבהם אדם מייצר את הפגם מעצמו וללא שירש את הפגם הגנטי מהוריו.(de novo)
מסיבה זאת העמותה ממליצה לשני ההורים לבצע את בדיקת הנשאות טרום הריון לשני ההורים. בדיקה אחת מכוסה בסל התרופות ועל השניה יש לשלם באופן עצמאי סכום של עשרות שקלים בלבד.
בנוסף, אפשרויות הטיפול הקיימות יכולות ליצור שיפור עצום בחיי הילדים החולים – שיפור שגדל ככל שהטיפול ניתן מוקדם יותר ולפני שנגרם נזק לעצבים השולטים בשרירי הגוף. לכן, לצד בדיקות טרום הריון, העמותה ממליצה לערוך בדיקת אבחון מוקדם לילוד כחלק מהבדיקות שנעשות לרכים הנולדים – בייחוד להורים שאחד מהם מזוהה כנשא SMA, כדי לאפשר התחלה מוקדמת ככל האפשר של הטיפול וקבלת תוצאות אופטימליות וצמצום למינימום את הפגיעה בבריאות ובאיכות החיים של הילדים.
במקרים בהם נשאות ההורים מזוהה במהלך ההריון, ניתן לערוך גם בדיקת SMA לפני הלידה, כחלק מבדיקת מי השפיר שנערכת לנשים לאחר השבוע ה-14 להריון או בבדיקת סיסי שלייה שבה נוטלים דגימת תאים מהשלייה בין השבוע ה-1 לשבוע ה-13 להריון.
יש להתייעץ עם הצוות הרפואי לגבי מידת נחיצות הבדיקות.
בדיקות הסקר המשמשות כיום מאפשרות לזהות רק 95% מכלל מקרי הנשאות לגן הגורם לSMA, ובאחת מכל 2,400 לידות שבהן רק אחד מההורים נשא מזוהה, עלול להיוולד ילד עם SMA.
מסיבות אלה, ובייחוד במקרים בהם אחד מההורים נשא מזוהה או שלא נעשות בדיקות טרום הריון, מומלץ לערוך לתינוקות הנולדים בדיקת אבחון מוקדם זמן קצר ככל הניתן לאחר הלידה.
הבדיקה נעשית, כמו בדיקות אחרות שנערכות כיום לתינוקות לאחר הלידה, בבדיקה של כמות זעירה של דם שנלקח מהעקב. תינוקות שנמצאים חיוביים בבדיקות הסקר נשלחים לבדיקות מעמיקות יותר.
בשנים האחרונות התחוללה מהפכה של ממש באפשרויות הטיפול הקיימות לילדים עם SMA, והן מאפשרות לילדים להגיע לרמות תפקוד שבעבר נחשבו דמיוניות בלבד – אולם יעילותם של הטיפולים עולה ככל שהתחלת הטיפול נעשית מוקדם ככל האפשר לאחר הלידה ולפני התפתחותם של תסמיני המחלה.
אבחון עם SMA יכול לעורר חרדות ולהביא לחוסר ודאות רבה. גורמים רבים יכולים להשפיע על האופן שבו המחלה תשפיע על הילד המאובחן ועל משפחתו, בהם מועד האבחון ותחילת הטיפול.
מחלת SMA היא הראשונה בעולם, שנמצאו לה 3 תרופות מצילות חיים ופורצות דרך, המבוססות על טכנולוגיות מתקדמות שפותחו במשך שלושה עשורים. שלוש התרופות המתקדמות זמינות במסגרת סל התרופות.
מלבד טיפולים אלה, ישנם אתגרים גופניים ובריאותיים שונים ודרכים שונות בהם ניתן לשפר את איכות חייהם של החיים עם SMA, כולל הקפדה על תזונה נכונה, פיזיותרפיה,תמיכה נשימתית ועוד.
הטיפולים החדשניים הזמינים כיום יכולים להביא לשיפור משמעותי במצבם של החיים עם SMA, בייחוד כשהם ניתנים בשלב מוקדם ולפני התפתחות תסמיני המחלה. אצל ילדים עם SMA, המחסור בחלבון הSMN גורם לתאי העצב השולטים במערכת השרירים להתנוון, וכאשר תא עצב מת, הוא לא מתחדש ואין לו תחליף. עבור ילדים עם הצורה החריפה ביותר של SMA, תשעה מכל עשרה מתאי העצב השולטים במערכת השרירים עלולים למות לפני הגיעם לגיל חצי שנה.
מתן מוקדם של הטיפול היא הדרך היחידה לעכב ולמנוע את אובדן תאי העצב ואת הפגיעה החמורה בשרירים וביכולת התנועה של הגוף.
במקרה של אבחון לאחר הלידה, מומלץ להתחיל את הטיפול מוקדם ככל האפשר – רצוי לפני הופעת תסמיני המחלה הראשונים. מחקרים שבחנו את הטיפולים השונים הראו כי ככל שהטיפול ניתן מוקדם יותר, כך תוצאותיו היו טובות יותר.
נכון לעכשיו, שלושה טיפולים מגבירי SMN מאושרים על ידי מנהל המזון והתרופות האמריקאי (FDA) וניתנים ללא עלות לכל חולי ה- SMA בישראל במסגרת סל שירותי הבריאות הממלכתי. החלטה על הטיפול המתאים מבין השלושה צריכה להתקבל ביחד בין המטופל/המשפחה לבין נוירולוג מומחה.
הטבלה שלהלן מתארת את הטיפולים הללו:
לאנשים החיים עם SMA מומלצת גישת טיפול רב תחומי, הכוללת מגוון מומחים רפואיים כל אחד לפי צרכיו. גישה כזו תסייע בשיפור הבריאות הכללית ואיכות החיים
הוועדה הבינלאומית לקביעת סטנדרט טיפולי עבור SMA הוקמה בשנת 2004 במטרה לקבוע הנחיות לגבי תקני טיפול SMA.
בשנת 2007 היא פירסמה הצהרת קונצנזוס לטיפול ב SMA, העוסקת בהיבטים שונים של אבחון וניהול, תוך התמקדות בשיקום וטיפול אורטופדי, ריאתי, תזונתי ופליאטיבי.
מסמך סטנדרט טיפולי מעודכן פורסם בשנת 2018, המשקף התקדמות חדשה בטיפול SMA.
ההנחיות מקדמות גישה רב-תחומית כמרכיב מרכזי בטיפול באנשים עם SMA, וממליצות לגבש צוות רחב של מומחים רפואיים בהקדם האפשרי. תוכנית טיפול צריכה להיות מתואמת על ידי ספק שירותי בריאות, בדרך כלל נוירולוג, הבקיא במחלה ומסוגל לספק טיפול פרואקטיבי לפי הצורך.
https://www.nmd-journal.com/article/S0960-8966(17)31290-7/fulltext
https://www.nmd-journal.com/article/S0960-8966(17)31284-1/fulltext
ריכזנו עבורכם את פרטי הקשר של המרפאות הרב- צוותיות המתמחות בטיפול בחולי SMA.
המרפאה הרב תחומית לחולי SMA הפועלת בבית החולים איכילוב מטפלת בתינוקות, ילדים וצעירים החולים במחלה ומרכזת את מרבית החולים בישראל. למרפאה מגיעים החל משלב האבחון, דרך קבלת תרופות וטיפולים גנטיים חדשניים ועד למעקב קליני הדוק, תמיכה בחולה ומשפחתו וליווי של עובדת סוציאלית. לאחר בדיקה גנטית, קלינית, מעבדתית והערכה פיזיותרפית צוות המרפאה ממליץ על טיפול רב-תחומי ומיטבי לחולה. הטיפול בחולי SMA הינו מורכב ומאתגר ולכן המרפאה פועלת בגישה רב תחומית מבוססת מומחים מתחום ריאות, אורתופדיה, אנדוקרינולוגיה, גסטרואנטרולוגיה, פיזיותרפיה ועוד. אנו פועלים בגישה של טיפול מקיף תוך שיתוף פעולה על מנת לתת למטופל טיפול מיטבי בכל ההיבטים של מצבו. המטופלים נמצאים במצבים מורכבים עקב אופי ומהלך המחלה. חלקם מונשמים ואינם ניידים ועל מנת להקל על ההתנהלות בכל ביקור, הצוות הרב תחומי מגיע אל המטופלים ולא להיפך.
אצל רובם המכריע של המטופלים נצפה שיפור קליני תודות לטיפול התרופתי, המעקב הקבוע והמענה המהיר לכל בעיה רפואית או אחרת שעולה.
בין צוות המרפאה והחולים ומשפחותיהם נוצרו קשרים מבוססי אמון, שיתוף פעולה והערכה אשר ללא ספק מסייעת ותורמת לרווחתם הנפשית והפיזית.
הטיפולים הניתנים במסגרת המרפאה הינם:
ספינרזה – הטיפול ניתן אינטראטקלי במינון אחיד שאינו תלוי בגיל ובמשקל. בשנה הראשונה 6 פעמים ולאחר מכן כל 4 חודשים לכל החיים.
זולג'נסמה – הטיפול ניתן למטופלים עד גיל שנתיים במתן תוך ורידי חד פעמי. המינון נקבע על פי משקל הילד.
ריסדיפלם – התרופה ניתנת מגיל חודשיים בצורה של תמיסה לשתייה במתן פומי פעם ביום בשעה קבועה לכל החיים. המינון משתנה בהתאם לגיל ומשקל המטופל.
ימי פעילות: המרפאה הרב תחומית ל SMA פועלת בימי שלישי.
ד"ר ליאורה שגיא – מנהלת מרפאת SMA
ד"ר רויטל לביא – נוירולוגית ילדים בכירה, מרפאת SMA
אנה שטמלר – אחות מרפאת SMA
פרופ' אביבה פתאל-ולבסקי – מנהלת המכון לנוירולוגיה ילדים
בטלפון 03-6947333
בין השעות 12:30-14:30
מענה בדוא"ל sma@tlvmc.gov.il יינתן תוך 3 ימי עבודה.
או בפקס 03-6974100
במרפאת SMA רב צוותית בשניידר מטפלים בילדים ונוער עד גיל 21 שנים. מטופלים שכבר אובחנו בשניידר ממשיכים בשלב זה מעקב גם בגיל בוגר יותר.
במסגרת המרפאה ניתנן מענה רב תחומי בד"כ כולו ביום אחד.
טיפולים חדשניים:
טיפול גנטי בזולגנסמה,
טיפול בספירנזה (גם מקרים מורכבים תחת שיקוף)
וכן טיפול פומי בריזדיפלם.
מנהלת המרפאה – ד"ר שרון אהרוני.
אחות מתאמת: תמי תעיזי.
רופאים נוספים:
ד"ר חגית לוין – רופאת ראות, מנהל שירות חולים מונשמים
פרופ' יורם נבו- נוירולוג
ד"ר שני לנדו-דותן – נוירולוגית
ד"ר רחל בלו – בריאות העצם
ד"ר נעמה אורנשטיין – גנטיקה
ד"ר אליהו פרלוב- רדיולוג פולשני
ד"ר ילנה צייטלין- רופאה מרדימה
ד"ר קונסטנטין ניקרסוב- רופא מרדים
אנשי צוות פרא- רפואיים:
פזיותרפיסטים: תניה מוס, תמי שניידרמן, צבי עטקין
פזיותרפיסטים נשימתיים: הדס מנטין, ניר הלפרין
מרפאות בעסוק: יולאינה אשל, ענבל קלם
קלינאית תקשורת: אושרת סלע- וייס
דיאטנית: יפעת פיש
עובדת סוציאלית: נועה אלבריט
מתאמות מחקר: יערה דאוד, הדס סולומון.
יצירת קשר דרך מזכירת המרפאה אורית רוקח
בטלפון: 03-9253615
במייל: neuro2@clalit.org.il
המרפאה למטופלים בוגרים עם SMA, בגילאי 18 ומעלה, פועלת במסגרתה הנוכחית בבית החולים איכילוב מזה למעלה 5 שנים. המרפאה מרכזת את מרבית החולים הבוגרים בישראל ומהווה אחת המרפאות הגדולות הגדולות באירופה. למרפאה מגיעים החל משלב החשד הקליני והבירור, דרך האבחון וקבלת תרופות וטיפולים חדשניים.
לאחר בדיקה גנטית, קלינית, מעבדתית, נשימתית והערכה נוירולוגית, צוות המרפאה ממליץ על טיפול רב-תחומי ומיטבי למטופל בהתחשב בצרכיו, אורח חייו וציפיות שלו לעתיד. הטיפול ב SMA הינו מורכב ומאתגר ולכן צוות המרפאה מורכב מנוירולוגים מומחים, המנוסים בתחום מחלות הנוירון המוטורי וב-SMA בפרט, עם ניסיון אבחוני וטיפולי רב שנים בתחום והכשרות בינלאומיות.
SMA בבגרות ובגיל המבוגר מצריך התייחסות לנושאים מורכבים והתמודדויות פיזיות, סוציאליות ורפואיות, שלרובנו מתחילות משנות העשרים ומאוחר יותר עם מצבים רפואיים נלווים.
בהבנה של מורכבות זו, הצוות מבוסס על מומחי נוירולוגיה של מבוגרים עם ניסיון בתחום ותוך התייחסות למורכבות החיים הבוגרים וכן תכנון משפחה ופוריות. אנו דוגלים במעקב קליני הדוק, הכרות וקשר רציף עם מטופלינו ותמיכה במטופל ומשפחתו עם הכוונה וליווי. קשר מבוסס אמון, שתוף פעולה ושקיפות – בתפישתנו, מסייעים ותורמים לרווחה הנפשית והפיזית.
הטיפולים הניתנים במסגרת המרפאה הינם:
ספינרזה – הטיפול ניתן אינטראטקלי במינון אחיד שאינו תלוי בגיל ובמשקל. בשנה הראשונה 6 פעמים ולאחר מכן כל 4 חודשים לכל החיים.
ריסדיפלם – התרופה ניתנת מגיל חודשיים בצורה של תמיסה לשתייה במתן פומי פעם ביום בשעה קבועה לכל החיים. המינון משתנה בהתאם לגיל ומשקל המטופל.
ד"ר יערה פיינמסר – מנהלת מרפאת SMA בוגרים מרכז רפואי ת"א ע"ש סוראסקי
דוא״ל
SMAclinic@tlvmc.gov.il
בבית חולים סורוקה פועלת מרפאה רב תחומית, רב גילאית לטיפול בחולי( SPINAL MUSCULAR ATROPHY ) SMA . את המרפאה מנהלת ד"ר איריס נוימן יחד עם ד"ר יעקב ביסטריצר (נוירולוג ילדים) וד"ר יאנה מצ'ניק סטין (נוירולוגית מבוגרים) העוסקים בתחום רפואת השריר.
המרפאה מעניקה טיפול רב תחומי לחולי SMA מהלידה ועד הבגרות (כל הגילאים). הטיפול התרופתי כולל את כל התרופות המאושרות בסל הבריאות ותרופות הניתנות כטיפול תומך על פי שיקול דעת המומחה. טיפול שאינו תרופתי כולל את המקצועות הטיפוליים.
שותפים למרפאה מומחים במקצועות נוספים הן בילדים והן במבוגרים רופאים מתחום ריאות ושינה, התפתחות הילד, טיפול נמרץ, זיהומיות, אא"ג, גסטרואנטרולוגיה, אורטופדיה, אנדוקרינולוגיה הרדמה וגנטיקה. פיזיוטרפיה – משקמת ומשמרת ופיזיוטרפיה נשימתית.
בילדים המרפאה עובדת בשיתוף עם המכון להתפתחות הילד בסורוקה ומעניקה לילדים אבחונים וטיפולים פרא רפואיים בתחומי הפיזיותרפיה, ריפוי בעיסוק וקלינאות תקשורת. עו"ס המלווה עו"ס העוזרת בתמיכה בחולים ובני משפחותיהם. קיים קשר הדוק מול היחידה לטיפול בבית ומעקב אחר מונשמי בית בקהילה.
ייחודה של המרפאה בהתאמת הטיפול לחולה ולמשפחתו ובמעבר בין מרפאת הילדים למבוגרים תחת אותה קורת גג ובקשר ההדוק שיש לנו מול הקהילה והטיפול בבית לחולי הנגב.
מזכירת היחידה לנוירולוגית ילדים – יסמין,
בטלפון: 08-6244650
מייל: somr63@clalit.org.il
מנהל המרפאה: ד"ר אמיר דורי
רופאים נוספים במרפאה:
ד"ר ורה ניקיטין – רופאה מומחה בנוירולוגיה
ד"ר מירב בן-דוד – מומחית במחלות עצב שריר
רופאים משתלמים בתחום מחלות עצב-שריר:
ד"ר עינת שקד – רופאה מומחית בנוירולוגיה
ד"ר אירינה צירקין – רופאה מומחית בנוירולוגיה
ד"ר מלאניה דומינקו – רופאה מומחית בנוירולוגיה
למרפאה מתקבלים מטופלים בני 18 ומעלה
הטיפולים הניתנים במסגרת המרפאה:
ספינרזה וריסדיפלם
דוא״ל
Neurology.mirp@sheba.gov.il
את המרפאה מרכזת נוירולוגית הילדים ד"ר טליה דור.
בצוות שותפים מומחים בתחומי:
ריאות – ד"ר ראובן צברי
קרדיולוגיה – ד"ר דין נחמן
אנדוקרינולוגיה – ד"ר ערן לביא
אורתופדיה – ד״ר שרודר
בנוסף, צוות פארא-רפואי הכולל פיזיותרפיסטיות ועובדת סוציאלית.
הטיפול מותאם לכל חולה בהתאם לגילו ולמצבו התפקודי.
למרפאה מתקבלים מטופלים בני 18 ומעלה
במרפאה מטפלים בכל התרופות הכלולות בסל התרופות המיועדות לחולי SMA.
ימי הפעילות:
ימי חמישי פעמיים בחודש.
במייל: yosefa@hadassah.org.il
או בטלפון: 02-5844751
עיצוב אתר: סטודיו שגב טל